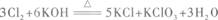
若有2 mol还原剂被氧化,则有 mol氧化剂被还原.
刷题刷出新高度,偷偷领先!偷偷领先!偷偷领先! 关注我们,悄悄成为最优秀的自己!
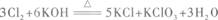
反应方程式为$\overset{- 1}{Cl_{2}} \longrightarrow \overset{- 1}{Cl^{-}} + \overset{+ 5}{ClO_{3}^{-}}$,根据方程式可以看出氯气既作为氧化剂又作为还原剂参与反应,氧化剂在反应中得到电子被还原,还原剂失去电子被氧化,氧化剂和还原剂的物质的量之比为生成物中化合价降低数值与升高数值之比的反比关系,也就是系数之比。反应中生成物系数之比为$KClO_{3}$:$KCl = 1:5$,即氧化剂与还原剂的物质的量之比为$5:1$。若有$2mol$还原剂被氧化,则有$5mol$氧化剂被还原。
本文链接:在以下的氧化还原反应中 若有2 mol还原剂被氧化,则有 mol氧化剂被还原.
版权声明:本站点所有文章除特别声明外,均采用 CC BY-NC-SA 4.0 许可协议。转载请注明文章出处。让学习像火箭一样快速,微信扫码,获取考试解析、体验刷题服务,开启你的学习加速器!
